PIからのメッセージ
2020年度版
がん研究を志す学生さんたちへ 2020年5月
 このホームページを読んでくださっている学生さんは、学部学生、修士課程大学院生、博士課程大学院生、あるいは、高校生かもしれません。いずれにしても今回のコロナ禍によって大変な忍従を強いられていると思います。まずは、皆さんの学業や研究活動が一日も早く再開することを祈ります。皆さん、大半の時間をご自宅や下宿で過ごされていると思います。私も最小限の研究活動のためにしか登所を許されておりませんので、会議あるいはスタッフや学生さんたちとの連絡は、専らメール、Facebook、リモート会議によって行い、多くの時間を、論文を書いたり読んだりあるいは何か考えたりということに使っております。リモート会議というのが大変便利で、同窓会をこれでやろうよという声が瞬く間に広まりまして、高校や中学の同級生と思いがけぬ時期に邂逅を果たすこととなりました。そこにはいろいろな職種で重要な地位を占めている人たちも参加していて、当然、今回のコロナ禍に話が及びます。そこで話したことのなかでとても印象深かったのは、このコロナ禍によって、自分が就いている職業の意味を期せずして問い直したということでした。社会活動が半ば麻痺した時に、自分の仕事の意味が改めて見えてきたということです。これを聞いたとき、やはり、私自身のことを考えました。私はがん研究者であり医師であります。まあ、今時医師が必要なのは、おそらく認めてもらえると思いますが、がん研究者のほうはどうだろうかと。我々の研究は10年とか20年後の癌治療の改善を目指します。いろんなことを調べてきていろんな提案をするわけですが、大半のアイデアやお薬は何の役にも立たずに消えていきます。現在SARS-CoV-2の実態解明や克服に取り組んでおられる感染症や公衆衛生の研究者からするとなんとも悠長な世界に見えると思います。
このホームページを読んでくださっている学生さんは、学部学生、修士課程大学院生、博士課程大学院生、あるいは、高校生かもしれません。いずれにしても今回のコロナ禍によって大変な忍従を強いられていると思います。まずは、皆さんの学業や研究活動が一日も早く再開することを祈ります。皆さん、大半の時間をご自宅や下宿で過ごされていると思います。私も最小限の研究活動のためにしか登所を許されておりませんので、会議あるいはスタッフや学生さんたちとの連絡は、専らメール、Facebook、リモート会議によって行い、多くの時間を、論文を書いたり読んだりあるいは何か考えたりということに使っております。リモート会議というのが大変便利で、同窓会をこれでやろうよという声が瞬く間に広まりまして、高校や中学の同級生と思いがけぬ時期に邂逅を果たすこととなりました。そこにはいろいろな職種で重要な地位を占めている人たちも参加していて、当然、今回のコロナ禍に話が及びます。そこで話したことのなかでとても印象深かったのは、このコロナ禍によって、自分が就いている職業の意味を期せずして問い直したということでした。社会活動が半ば麻痺した時に、自分の仕事の意味が改めて見えてきたということです。これを聞いたとき、やはり、私自身のことを考えました。私はがん研究者であり医師であります。まあ、今時医師が必要なのは、おそらく認めてもらえると思いますが、がん研究者のほうはどうだろうかと。我々の研究は10年とか20年後の癌治療の改善を目指します。いろんなことを調べてきていろんな提案をするわけですが、大半のアイデアやお薬は何の役にも立たずに消えていきます。現在SARS-CoV-2の実態解明や克服に取り組んでおられる感染症や公衆衛生の研究者からするとなんとも悠長な世界に見えると思います。
本邦において何の対策もとらぬ場合にCOVID-19で亡くなるひとは約42万人と北海道大学の先生が推定されておりました。がんで亡くなるひとは2018年の数字で年間約37万人です。がんの予防、診断、治療にはものすごい額の予算が投入される訳ですから、これと同程度の死者を出すかもしれないCOVID-19がいかに重要な政策課題であるかわかります。しかし、若い人たちからすると、若年齢者が滅多に亡くなることのないCOVID-19のために学校が閉まったり、バイトがなくなったり、コンサートにもレストランにも行けないし、就職もままならなくなるかもしれないというのは、ちょっぴり不満かもしれません。がんもこれとよく似ています。私が研究している網膜芽細胞腫は産まれてすぐの赤ちゃんにも発症しますし、これを含む小児がん、いわゆるAYA世代のがん、白血病、胃がん等々早くに発症するがんはたくさんありますが、大半は60代より後ろの世代の問題であります。現在の本邦のがん医療は、中央値でおおよそ60代の患者さんが治療開始して5年以上生存する確率を60%ほどに持ってきています。若年者に起きる希少がんにもっと研究者を投入しなければというムーブメントはかなり大きくなってきています。でも、加齢とともに蓄積するエラーがその引き金を引くというがんの本態を考えると、基本的にお年寄りの問題であることは変わることはないです。閣僚や国会議員の大半はご高齢なので、お金を出してくれるのでしょうか。でも、いろいろなひとと話をすると、「がんでは死にたくないなあ」というのが老若問わずに出てきます。がんと他の疾患の違いは何でしょう。
研修医を内科で行いましたので、悪性疾患、循環器疾患、代謝疾患、免疫疾患と様々な患者さんを受け持ちました。循環器科入院中の心筋梗塞の患者さんが心不全を起こした時は、その辺にいた研修医、看護師、上級医が病室になだれ込んできて処置を行い、不幸にして亡くなると、何事も無かったかのように平静の病棟にさっと戻ります。ところが、がんの患者さんがもう危ないというときは、その患者さんを受け持った歴代の研修医や主治医に連絡が行き、ベッドサイドに集まり、時間のある者は、家族の邪魔にならぬようにではありますが、心拍が停止するまで病室や詰め所にとどまりお見送りします。翌日、空になった病室の前に主治医がじっと立っていた姿を見たことがあります。急性疾患による死に比べると、その意味についてあらかじめよく考え、その完遂の様態を味わい噛みしめる機会が多いのががん死の特徴といえるかもしれません。多くの研修医がこういう経験を抱えて大学院での研究に挑戦するのではないでしょうか。私もその一人でした。ある時急性骨髄性白血病の患者さんが亡くなり、ご遺族の篤志により剖検をさせてもらえました。子宮に割面を入れたその刹那に怪しい緑色が現れました。緑色腫chloromaといって髄外臓器に浸潤した白血病細胞のプロトポルフィリンの代謝産物なんかが発色を示す現象です。不謹慎ではありますが、私は、これに一瞬みとれてしまいました。なんて神秘的なんだろう!と。その患者さんの血液標本は自分でストリッヒを引いて染色をしていましたので、末梢血中の白血病細胞(芽球)を経時的に観察しておりました。おまえはこんなことまでやっちゃうのかと感じた次第です。学部学生の頃もウイルス研究所というところで成人T細胞白血病を起こすウイルスの研究をしておりましたが、おそらくこの緑色腫を見てしまったことが、その後の身の振り方の決定に大きく影響したと思います。
じゃあ、がん研究ってなんなのか。仮にがん治療や研究を全く止めてしまったらどうなるか?がん治療を全くしなくなったらどうなるかなんて計算をいままで見たことはありません。でも、がんに対して人類が無力であった時代も人口は順調に増えた訳ですから、生物学的にはたいしたことは起こらぬかもしれません。平均余命は縮むでしょう。しかし、女性が今より多くの子供を産むことができれば、超高齢社会は解消され、健全な社会に復するのかもしれません。反対に、一生懸命働いたのだから少しでも長く余生を楽しみたい、家族内の年長者にできるだけ長生きしてもらいたいというというのもごく自然な欲求であります。がんとの闘いは、このように不条理なものであります。しかし、ニクソン大統領が1971年にがん対策法(がん戦争宣言)に署名し、1983年に中曽根首相が対がん10カ年総合戦略を策定、人類はがんを徹底的に知りこれと闘う方向に走り出したのであります。それが今、我々がん研究者にとってはいわば飯の種となっています。COVID-19に対して各国がいち早く準備を始めたのと同じように、人類は、がんとの闘いをほぼ自然に選択したわけです。
がん研究をするのは、医師でなくても全く問題ありません。私のところには、医学、薬学、生物学、農学、栄養学、と様々な分野出身のスタッフと学生が集っていて多様な見地から研究を行っています。がん研究とはなにか?という問いに対する答えも個人個人で全く違うはずです。いや、明確な答えを見つけているひとはあまりいないのではないでしょうか。私もまだ答えにはたどり着いていないと思います。ただ、研究をやり続けないと答えに行き着かぬであろうというのは感じます。私が学部学生の時「ウイルスとがん」(岩波新書)という本を読んで感動し著者のもとを訪ねました。どうやってがんを勉強するのがいいでしょうかという私の問いに対して著者が即座に返したのは「それは研究することだよ」という答えでした。その翌日から私の研究人生が始まり今に至っております。あなたも、がん研究をしてみませんか?
我々の最近のアプローチについて
金沢市の角間にあるがん進展制御研究所に新しくラボを構えて10年が経過しました。スタート時は、Ras、RECK、RB1という’R’がつく三つの遺伝子に注目しました。2020年現在は、研究標的をRB1に絞っています。RB1はクローニングから30年以上が経過したがん抑制遺伝子であります。ほぼすべてのがん化シグナルは、RB1がん抑制遺伝子がコードするタンパク質の働きにブレーキをかけることによって異常な細胞周期進行を促進します(図1)。また、RB1そのものの機能が喪失することによってもがんが生じたり悪性化したりします(図2)。我々は、RB1の機能が抑制された時に起こる様々な現象(未分化性亢進、治療耐性獲得など)の分子機構を詳細に調べることによって、がんの悪性進展に対抗する方法を研究してきました。その結果、RB1がまだ使えるがんともう使えなくなったがんに分けて治療法を考えるとよいという考えを持つに至りました。
RB1機能を保持しているがんの攻略
ほぼすべてのがん化シグナルは、D型サイクリンの発現を亢進することによってサイクリン依存性キナーゼ(CDK)群の働きを強め、RB1のモノリン酸化を誘導、これが、14箇所のリン酸化によるRB1の機能喪失の引き金となります。これまで使用されてきた分子標的薬(イレッサ、グリベック、トラメチニブなど)は、がん化シグナルを途中でブロックするものです。我々が今注目しているのは、CDK4とCDK6の活性を同時に阻害する薬剤です。これは、RB1のモノリン酸化を阻害することによって、RB1のがん抑制機能を取り戻させます。つまり、がん化シグナルの終着点を切ることによってがんを治療するやり方です(図1)。進行性のホルモン依存性乳がんに対し保険適用が認められていて、ホルモンの働きを弱める薬と併用することによって無病生存期間(DFS)を2倍に延長するなどの効果が見られています。我々は、CDK4/6阻害剤の適用拡大を念頭に、本剤効果の詳細な分子機序と内因性の耐性機序を解明しようとしています。
RB1機能を喪失したがんの攻略
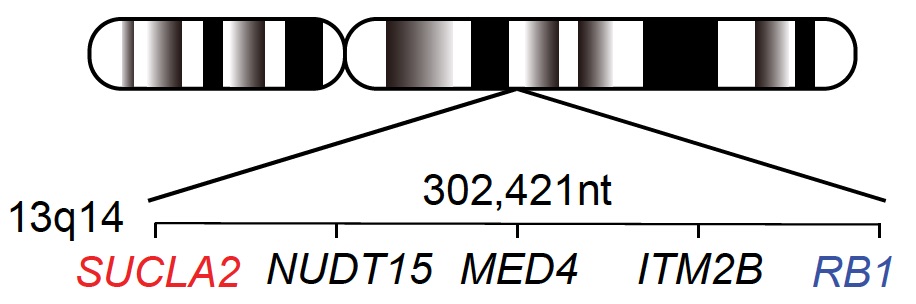
これは20年以上かけて研究してきました。RB1機能を喪失することによって、細胞周期進行が促進するだけでなく、Rasがん化シグナルが増強されることや、細胞内代謝(解糖系、脂質合成系)や腫瘍微小環境の改編が起こり、がん細胞の生存戦略が強化されることを明らかにしました。これまでに見つけたRB1標的分子のいくつかを新規治療標的としてインキュベートしております。最近、RB1機能喪失と合成致死性を示すAurora A/B、CHK1、PLK1などの分子にも注目しています。また、RB1遺伝子欠失を含むゲノム異常に巻き込まれることによって欠失するSUCLA2という代謝遺伝子にも着目しています(図3)。SUCLA2を欠失した進行前立腺がんを治療する薬剤を開発しています。
図1
ほぼすべてのがん化シグナルはRB1機能にブレーキをかける。
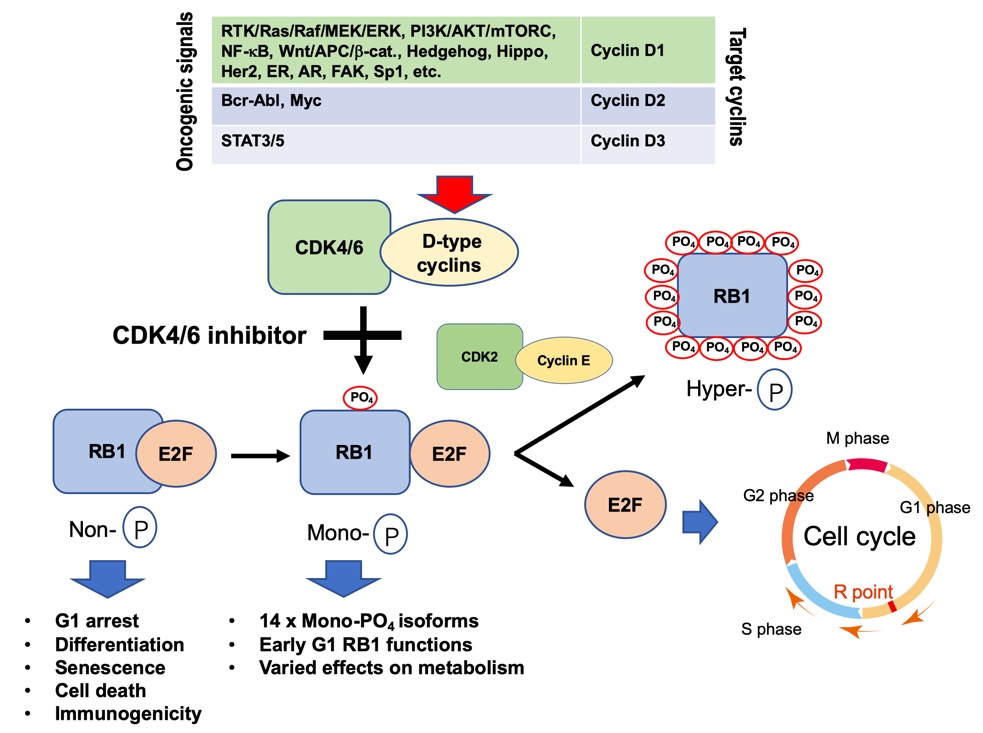
図2
RB1機能を抑えることによって生じた脳腫瘍(左)と肝臓がん(右)。
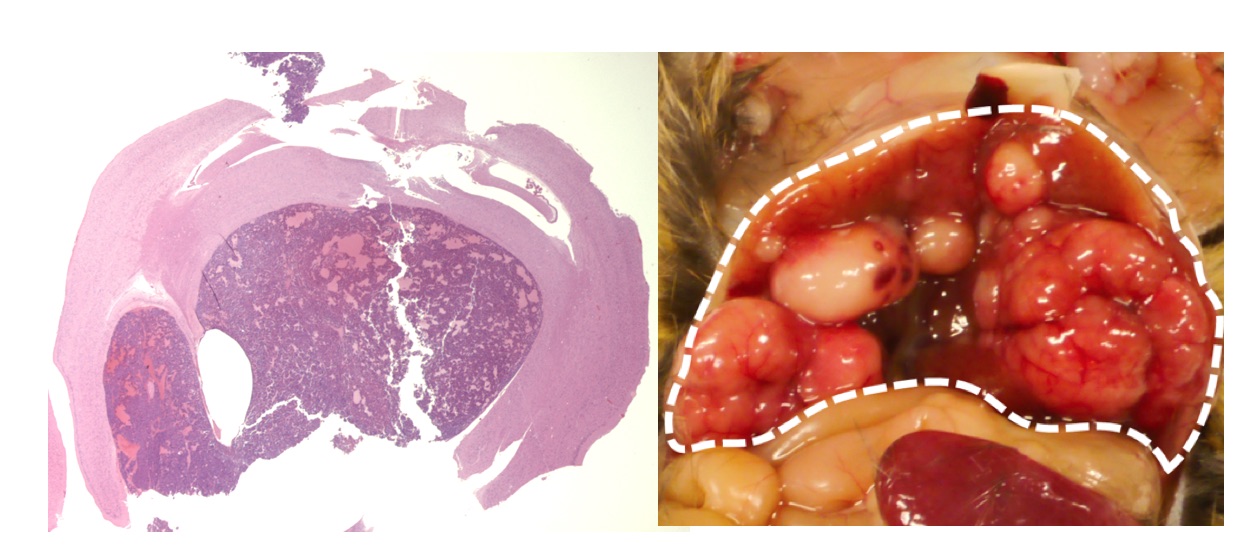
図3
RB1がん抑制遺伝子の近傍にあるSUCLA2代謝遺伝子の同時欠失はがん細胞のアキレス腱になる。
令和2年5月5日
髙橋智聡
2013年度版
 がんが遺伝子の病気であるという通念を決定的に裏付けしたのは、がん遺伝子・がん抑制遺伝子の同定であります。がんを引き起こすウイルスのもつ遺伝子とほぼ同じものがヒトのゲノム遺伝子中にも存在し、しかも、ヒトのそれは、わずか一カ所の突然変異によって細胞をがん化する。がん遺伝子は、このような経緯で発見され、すぐ後に訪れたがん抑制遺伝子の発見とともに、20世紀末のがん研究の爆発的な進展に大きく寄与しました。また、これらの遺伝子産物の働きを解明する努力は、生命科学全般を強力に牽引することになりました。
がんが遺伝子の病気であるという通念を決定的に裏付けしたのは、がん遺伝子・がん抑制遺伝子の同定であります。がんを引き起こすウイルスのもつ遺伝子とほぼ同じものがヒトのゲノム遺伝子中にも存在し、しかも、ヒトのそれは、わずか一カ所の突然変異によって細胞をがん化する。がん遺伝子は、このような経緯で発見され、すぐ後に訪れたがん抑制遺伝子の発見とともに、20世紀末のがん研究の爆発的な進展に大きく寄与しました。また、これらの遺伝子産物の働きを解明する努力は、生命科学全般を強力に牽引することになりました。
このように、がんに関する展望は、一遺伝子の所行というところまで還元・単純化され、その当時学生であった私も、これでがんは克服されるのだと考えました。しかし、現実には、そう簡単には行きませんでした。ヒトのゲノム中には、22,000種類以上(最大26,800とも)の遺伝子が含まれていると考えられています。これらの遺伝子は、様々な転写制御因子やnon-coding RNAによって、その発現の強弱やRNA安定性が制御されます。それだけでなく、エピジェネティック、つまり、DNA配列が変更されなくても、DNAそのものあるいはDNAを巻き付けているクロマチンへの様々な化学的修飾によって、遺伝情報の読み取られ方は、ダイナミックに変化します。
発がんにおけるはじめの一歩は、がん遺伝子・がん抑制遺伝子の活性の変化によって踏み出される場合が多いと思われますが、そうなった途端に、その細胞内で22,000種類以上の遺伝子のもつ意味(私はコンテクスト「文脈」と呼んでいます。)は変わります。そして、この文脈のなかで特別な意味を獲得した遺伝子の使われ方あるいは情報にさらなる異常が起こると考えています。私たちは、様々な「がん化の文脈」において特別な役割を果たす遺伝子を同定し、その働きを詳しく調べることによって、がんを克服するための戦略をたてようとしています。
RECKは、Rasにがん原性の突然変異が起こったときに発現が抑制され、しかし、強制発現するとRas突然変異によって誘導されるがんの挙動のいくつかを抑制する遺伝子産物として同定しました。私の研究グループは、さらに、RECKが、MT1-MMP、CD13/APN, ADAM10等の膜型メタロエンドペプチダーゼ群と相互作用することによって、がんの増殖(増殖シグナル、細胞周期)、浸潤・転移、腫瘍血管新生や大脳皮質発生を制御することを突き止めました。また、RECKは、様々な臨床がんの予後に影響を与えることが知られています。
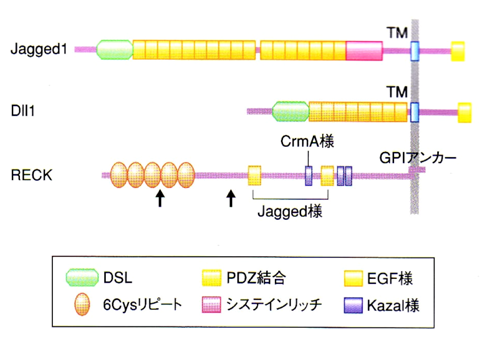
RECK蛋白質の一次構造とある種の蛋白質分解酵素阻害因子やNotchリガンドとの相同性。
矢印は、メタロエンドペプチデースへの阻害活性中心と考えている部位。
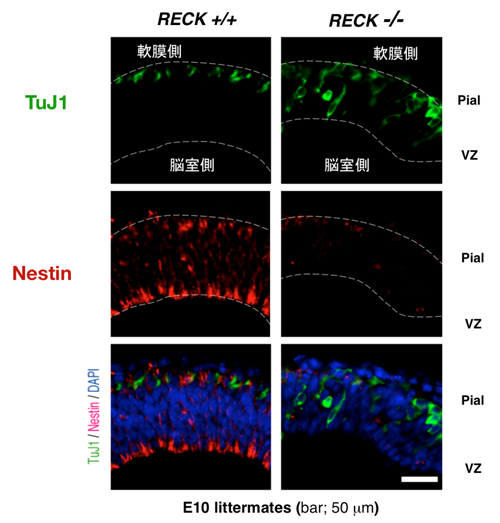
RECKノックアウトマウスの大脳において観察された神経前駆細胞の早熟分化。
RECK活性の消失は、Notchリガンドの過剰なシェディングを生じるために、
Notchシグナルを減弱させる。
この表現型は、Notchシグナルが途絶したマウスのそれとそっくりである。
次に、私たちは、Rbがん抑制遺伝子が不活性化するという「文脈」におけるRasプロトがん遺伝子の知られざる機能を明らかにしました。内在性のRasの活性は、細胞周期に依存して変化します。ところが、Rbが不活性化されると、このような周期性を喪失し、とくにN-Rasというアイソフォームの活性が上昇します。この研究を始めた頃は、RasはD型サイクリン群の転写調節によってRbのリン酸化を制御するということが知られていましたが、線虫の研究などから、逆に、RbがRas活性を制御する可能性も示唆されておりました。このがん抑制遺伝子とがん遺伝子のチャンピオンどうしの相互抑制的な遺伝学的関係は、科学的に大変興味深く、また、臨床的にも意義深いと考え、RbとRas遺伝子を両方欠くマウスをつくってみました。そこから様々な新しいことが判ってきたことは、また別の欄(研究内容)で詳説したいと思います。

RBとRasを結ぶ新しいパスウェイを発見するきっかけになった、線虫における知見。
線虫のRasの活性化変異は、vulva(陰門)の発生異常を生じる。
変異によってこれと同じ表現系を生じる遺伝子が探索され、RBが、その一つであることがわかった。
Mingxue Cui and Min Han, Worm Bookより改変。
現在は、上記の研究の過程で明らかになったRBの新規機能に焦点をあて、とくに、そのがん幹細胞における役割を追求しています。がん幹細胞は仮説的な存在でありますが、それが存在するとして研究を進めることが、がん治療戦略の飛躍的な発展に繋がると考えています。我々がこれまでに得た知見をもとに、安定で解析の容易な「インビトロがん幹細胞モデル細胞」を拵え、これをがん幹細胞出現・維持機構の解明と、あたらしいがん標的薬の開発につなげようと日々がんばっています。
さて、ここまで読んでいただくと、なんとなく感じていただけたかと思いますが、私たちのがん研究のスタイルは、特定のがん腫を扱うのではなく、臨床的レリバンスが高い(様々ながんにおいて重要な役割を果たすエビデンスが豊富な)遺伝子の働きに注目し、その時々の疑問に答えるためにもっとも便利な実験系を作製しながら、がんを克服する戦略を考えようとするものです。現在の私のグループには、内科出身(私)、外科出身、農学部出身、工学部出身、薬学部出身と、多彩なバックグラウンドをもつスタッフが集っております。多様かつ柔軟なアプローチによるがん研究を目指します。一緒に夢を追いかける仲間を捜しております。
一医師としてのがん研究
私は、医学部学生時代に基礎研究者としての修行をはじめました。岩波新書の「ウイルスとがん」を読んで、その著書である畑中正一先生(当時京都大学ウイルス研究所教授)に会いに行ったのです。がんを深く勉強するにはどうしたらよいかを教えてもらおうと思ったのです。ところが、その場で、放課後にアルバイトとして研究することが決まりました。教科書の勉強はあまり役に立たない、自分の手で研究をしないとだめだ、というのが、彼の主張でした。それからの日々がどんなに楽しかったか。中でも、成人T細胞白血病を引き起こすウイルスゲノムの中にほ乳類の細胞をトランスフォームする遺伝子Taxを同定した研究に参画し、これが大変有名な論文になったことが、私の後の生き方を決定しました。国家試験の勉強が切羽詰まる6年の早秋頃まで、実験をしていました。時代は、すでに、ウイルス発がんから内在性がん遺伝子へ、そして、がん抑制遺伝子へと動いておりましたが、これは、ヒトに白血病を起こすウイルスですから、インパクトは大きかったわけです。そこから逆に血液学に興味を持ち、研修医時代は、主に血液・消化器の悪性疾患の臨床の習得を目指しました。白血病の臨床では、若い人たちが治療の甲斐無く亡くなっていくこと、消化器の臨床では、手術適応の無い症例に対して打つ手がほとんど無いことを知りました。また、当時の基礎がん研究を席捲していたがん遺伝子やがん抑制遺伝子等の概念が、実際の臨床では、まだ何の役にも立たないことも身にしみてわかりました。悩んだ末に、基礎学問がしっかりと臨床の役に立つようになるまで、しばらくは基礎研究側に身をおくことにしました。ただ、常に、一医師として考え、研究の方向を選択する。このことだけは、心に誓っています。研修終了後、当時東京の上池袋にあった癌研究所の野田亮先生のラボで、Ras研究に身を投じました。Rasは、言うまでもなく、がん遺伝子のチャンピオンでありますし、血液・消化器の悪性疾患に深く関わります。また、シンプルながんモデルを組み立て、できるだけバイアスのかからないライブラリースクリーニングという手法を用いてがんを考えるという、臨床がんからはほぼ隔絶した研究手法が気に入り、その研究室を選びました。苦労も味わいましたが、Rasを切り口に、様々な研究分野との邂逅を果たしました。
金沢大学がん進展制御研究所について
私は、2009年12月に、四半世紀近くをそこで過ごした京都大学医学研究科を離れ、金沢大学がん研究所に着任いたしました。その後、2011年4月に金沢大学がん進展制御研究所に改称・改組となり、がんの悪性進展機構の深い理解と転移・浸潤・再発の克服を目指す国立大学附置研究所として、ますます充実した研究を推進するとともに、全国共同利用・共同研究拠点の一角として、幅広い分野での研究ネットワークの構築を目指しております。この研究所には、清木・佐藤博士らによるMT1-MMPの発見をはじめ、世界に誇ることのできる数々の業績があり、現在も、若い教授を中心に、活発な研究活動が繰り広げられております。毎月行われるOncology Seminarでは、研究室の垣根を越えて、活発な意見交換がなされます。研究設備は、がん研究のほとんどのニーズに対応しています。研究環境と住環境は、全国屈指であると言って差し支えないでしょう。都会暮らしに疲れ果てながら研究するより、金沢の穏やかに流れる時間のなかで、じっくりと腰を落ち着けて研究するのもよいかもしれません。当研究室は、大学院生の受け入れを積極的に行っております。大学院制度は、金沢大学大学院医薬保健学総合研究科の医学博士課程および医学修士課程、または、理工学域自然システム学類バイオ工学コース博士課程前期を利用することが可能です。医薬保健学総合学科博士課程学生向けに、がん研独自の奨学制度も整備しております。

研究室の窓からの夏と冬の風景。

2011年の新人歓迎会。